 |
| ▲14일 서울 강남구 코엑스 Hall A에서 열린 '제35회 국제의료기기·병원설치 전시회(KIMES)'의 재활 의료기기 부스 직원들이 재활운동을 시연하고 있는 모습. |
[일요주간 = 노현주 기자] 인공지능(AI)·3D 프린팅·로봇 등 혁신 의료 기술의 시장 조기 진입이 가능해졌다.
보건복지부는 14일 ‘혁신의료기술 별도평가트랙’ 도입 및 ‘신의료기술 평가기간 단축’의 내용을 담은 신의료기술평가에 관한 규칙 개정안을 15일부터 시행한다고 밝혔다.
정부는 지난해 7월 ‘의료기기 규제혁신 및 산업육성방안’을 통해 AI와 3D 프린팅, 로봇 등 첨단기술이 융합된 혁신의료기술에 대해서는 기존의 의료기술평가 방식이 아닌 별도의 평가트랙을 도입하겠다고 발표했었다.
복지부는 지난해 9월부터 ‘혁신의료기술 별도평가트랙’ 시범사업을 추진했고, 그 결과를 바탕으로 신의료기술평가 규칙 개정안을 마련했다.
개정된 주요 내용을 보면 우선 첨단기술이 융합된 의료기술과 암과심장질환 등 사회적 활용가치가 높은 의료기술은 기존의 신의료 기술평가가 아닌 별도 평가트랙을 활용할 수 있게 된다.
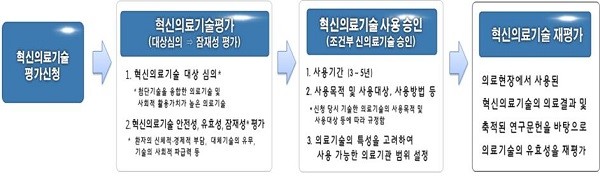 |
| ▲ 혁신의료기술 별도평가트랙 절차 |
그동안 출판된 문헌을 근거로 의료기술의 안전성과 유효성을 평가했던 신의료 기술평가는 새로운 의료기술이 현장에 사용되기 전 기본적인 안전성과 유효성을 폭 넓게 검토한다는 장점이 있었다.
그러나 의료기술이 빠르게 변화하는 환경 속에서 혁신적인 의료기술의 현장 활용을 지체시켜 의료기술 발전을 저해할 수 있다는 지적도 있었다.
복지부와 한국보건의료연구원은 의료기술의 사회적 가치와 잠재성을 평가하는 방법을 연구해 기존의 문헌 중심의 평가체계를 보완하는 ‘잠재성 평가방법’을 개발했다.
이번에 도입되는 ‘혁신의료기술 별도평가트랙’에서는 기존의 문헌 평가와 함께 새로 개발된 의료기술의 잠재성 평가까지 진행한다.
기존의 평가체계에서 유효성을 평가할 문헌이 부족해 탈락했던 의료기술 중 환자의 삶을 획기적으로 개선하거나 환자의 비용 부담을 줄여주는 등 높은 잠재성을 가졌을 경우 조기 시장 진입이 허용된다.
다만, 혁신의료기술이라 해도 사람의 인체 조직 내부에 행해지는 의료행위로 환자의 부담이 큰 의료기술에 대해서는 문헌을 통한 엄격한 안전성 검증을 실시한다.
또 ‘혁신의료기술 별도평가트랙’을 통해 의료현장에 도입된 혁신의료기술은 의료현장에서 활용된 결과를 바탕으로 3~5년 후 재평가를 받아야 한다.
이를 위해 혁신의료기술을 개발한 의료기기 업체 등은 이를 사용하는 의료기관 및 실시 의사, 재평가를 위해 수집되는 자료 등을 한국보건의료연구원에 제출해야 한다.
허위로 자료 제출을 하거나 허용된 의료기관 이외에서 의료기술을 사용하면 혁신의료기술의 사용이 중단될 수 있다.
지난해 7월 의료기기 규제혁신 방안에 포함된 것처럼 신의료 기술평가의 기간도 30일 단축된다.
이를 위해 전문가 서면 자문을 통해 신의료 기술평가 대상 여부를 판단했던 절차를 내부 평가위원으로 대체해 2단계의 평가절차를 1단계 평가절차로 줄인다. 이로 인해 외부 전문가 탐색·구성 등에 발생했던 시간을 절약해 평가기간이 250일로 단축된다.
손호준 복지부 의료자원정책과장은 “혁신의료기술 별도평가트랙의 도입으로 그간 늦어졌던 혁신의료기술의 활용을 촉진하되 의료기술의 안전성은 엄격히 검증할 것”이라며 “신의료기술 평가기간을 단축해 다소 긴 평가기간으로 인해 어려움을 호소했던 의료기기 업체들의 부담도 줄어들 것”이라고 말했다.
'시민과 공감하는 언론 일요주간에 제보하시면 뉴스가 됩니다'
▷ [전화] 02–862-1888
▷ [메일] ilyoweekly@daum.net
[저작권자ⓒ 일요주간. 무단전재-재배포 금지]































































![부산 덕포동 중흥S클래스 건설현장서 화재 발생...검은 연기 치솟아 [제보+]](/news/data/20220901/p1065590204664849_658_h2.jpg)
![[포토] 제주 명품 숲 사려니숲길을 걷다 '한남시험림'을 만나다](/news/data/20210513/p1065575024678056_366_h2.png)
![[포토] 해양서고 예방·구조 위해 '국민드론수색대'가 떴다!](/news/data/20210419/p1065572359886222_823_h2.jpg)
![[언택트 전시회] 사진과 회화의 경계](/news/data/20210302/p1065575509498471_939_h2.jpg)










